No tiene ningún artículo en su cesta
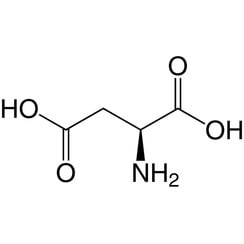
Ácido aspártico
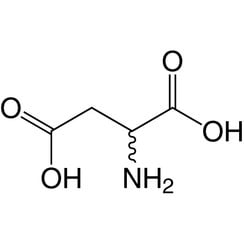
El ácido aspártico (símbolo Asp o D; su forma iónica se conoce como aspartato), es un α-aminoácido utilizado en la biosíntesis de proteínas. Como todos los aminoácidos, contiene un grupo amino y un ácido carboxílico. El grupo α-amino se encuentra en el –NH + protonado
3 se forma en condiciones fisiológicas, mientras que su grupo ácido α-carboxílico se desprotona -COO- en condiciones fisiológicas. El ácido aspártico tiene una cadena lateral ácida (CH2COOH) que reacciona con otros aminoácidos, enzimas y proteínas del cuerpo. En condiciones fisiológicas (pH 7,4) en las proteínas, la cadena lateral suele presentarse como la forma de aspartato cargada negativamente, −COO -. [5] Es un aminoácido no esencial en los seres humanos, lo que significa que el cuerpo puede sintetizarlo según sea necesario. Está codificado por los codones GAU y GAC.
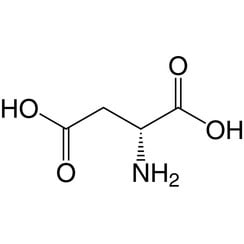
El D-aspartato es uno de los dos D-aminoácidos que se encuentran comúnmente en los mamíferos.
En las proteínas, las cadenas laterales de aspartato a menudo se unen al hidrógeno para formar giros asx o motivos asx, que a menudo ocurren en los extremos N de las hélices alfa.
El isómero L de Asp es uno de los 22 aminoácidos proteinogénicos, es decir, los componentes básicos de las proteínas. El ácido aspártico, al igual que el ácido glutámico, se clasifica como un aminoácido ácido, con un pKa de 3,9, pero en un péptido depende en gran medida del entorno local y puede llegar a 14. Asp es omnipresente en la biosíntesis. Dado que el cuerpo puede producir aspartato, se clasifica como un aminoácido no esencial.