No tiene ningún artículo en su cesta
Sulfato de amonio y hierro (II)
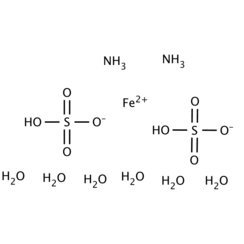
El sulfato de amonio y hierro (II) o la sal de Mohr es el compuesto inorgánico con la fórmula (NH4) 2Fe (SO4) 2 (H2O) 6. Contiene dos cationes diferentes, Fe2 + y NH4 +, y se clasifica como una sal doble de sulfato ferroso y sulfato de amonio. Es un reactivo de laboratorio común porque cristaliza fácilmente y los cristales resisten la oxidación por el aire. Al igual que las otras sales de sulfato ferroso, el sulfato de amonio ferroso se disuelve en agua para obtener el aquocomplejo [Fe (H2O) 6] 2+, que tiene geometría molecular octaédrica. La forma mineral es mohrite.
En química analítica, esta sal es la fuente preferida de iones ferrosos porque el sólido tiene una vida útil prolongada y es resistente a la oxidación. Esta estabilidad se extiende un poco a las soluciones que reflejan el efecto del pH sobre el par redox ferroso / férrico. Esta oxidación ocurre más fácilmente a pH alto. Los iones de amonio hacen que las soluciones de la sal de Mohr sean ligeramente ácidas, lo que ralentiza este proceso de oxidación. El ácido sulfúrico a menudo se agrega a las soluciones para reducir la oxidación a hierro.
Se utiliza en el dosímetro Fricke para medir altas dosis de radiación gamma.