Il n'y a aucun article dans votre panier
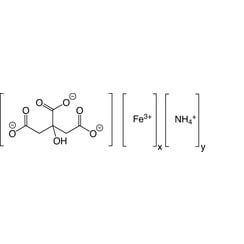
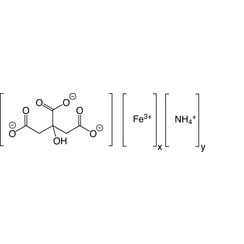
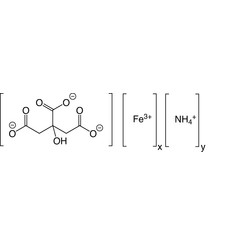
Citrate d'ammonium et de fer (III)
Le citrate d'ammonium et de fer (III), également connu sous le nom de citrate de fer d'ammonium, de citrate de fer et d'ammonium, de citrate d'ammonium ferrique ou de fer citrique, se forme de manière non stoechiométrique, en fonction de la teneur en fer du vert (14,5 à 16% Fe) à brun (16,5 à 28% Fe) dans l'eau cristaux solubles qui sentent légèrement l'ammoniaque. Les cristaux, qui sont peu solubles dans l'éthanol, se dissolvent dans l'air et se décomposent par la lumière (du soleil).
Il est principalement utilisé pour la photosensibilisation. Les tissus imprégnés de solutions de citrate de fer ammoniacal, d'acide tartrique et de nitrate d'argent peuvent être utilisés comme photo-positifs avec des nuances de brun.
Le citrate d'ammonium et de fer (III) est utilisé à la fois en cyanotype et en médecine, ici pour le traitement de l'anémie ferriprive.
-Autres utilisations
-En tant qu'additif alimentaire, où il porte le numéro E E381, et est utilisé comme régulateur d'acidité. Notamment utilisé dans la boisson écossaise Irn-Bru.
-Purification de l'eau.
-En tant qu'agent réducteur de sels métalliques peu actifs tels que l'or et l'argent.
-Avec ferricyanure de potassium dans le cadre du processus photographique cyanotype.
-Utilisé dans les profondeurs de fer Kligler pour déterminer la production de sulfure d'hydrogène dans le métabolisme microbien.
-En imagerie médicale, le citrate de fer ammoniacal est utilisé comme agent de contraste.
- Comme hématine.