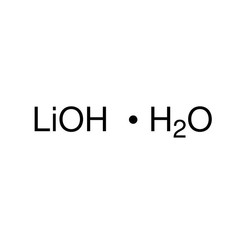U heeft geen artikelen in uw winkelwagen
Lithiumhydroxide
Lithiumhydroxide is een anorganische verbinding met de formule LiOH. Het is een wit hygroscopisch kristallijn materiaal. Het is oplosbaar in water en lichtjes oplosbaar in ethanol, en is commercieel verkrijgbaar in watervrije vorm en als monohydraat (LiOH.H2O). Hoewel lithiumhydroxide een sterke base is, is het het zwakste bekende alkalimetaalhydroxide.
Toepassingen
Lithiumhydroxide wordt voornamelijk verbruikt bij de productie van lithiumvetten. Een populair lithiumvetverdikkingsmiddel is lithium 12-hydroxystearaat, dat een algemeen smeervet produceert vanwege de hoge weerstand tegen water en de bruikbaarheid bij verschillende temperaturen.
-Kooldioxide schrobben
Lithiumhydroxide wordt gebruikt in ademgaszuiveringssystemen voor ruimtevaartuigen, onderzeeërs en rebreathers om kooldioxide uit uitgeademd gas te verwijderen door lithiumcarbonaat en water te produceren:
2 LiOH • H2O + CO2 → Li2CO3 + 3 H2O
of
2 LiOH + CO2 → Li2CO3 + H2O
Dit laatste, watervrij hydroxide, heeft de voorkeur vanwege zijn lagere massa en lagere waterproductie voor ademhalingssystemen in ruimtevaartuigen. Een gram watervrij lithiumhydroxide kan 450 cm3 kooldioxidegas verwijderen. Het monohydraat verliest zijn water bij 100–110 ° C.
-Andere gebruiken
Het wordt gebruikt als medium voor warmteoverdracht en als elektrolyt voor accu's. Het wordt ook gebruikt in keramiek en sommige Portland-cementformuleringen. Lithiumhydroxide (isotopisch verrijkt met lithium-7) wordt gebruikt om het reactorkoelmiddel te alkaliseren in reactoren onder druk voor corrosiecontrole.