Keine Artikel in Ihrem Warenkorb
Phosphorpentoxid
Phosphorpentoxid, genauer Diphosphorpentoxid, ist ein Oxid des Elementes Phosphor und gehört zur Stoffgruppe der Phosphoroxide. Es ist ein farb- und geruchloses, äußerst hygroskopisches Pulver, das mit Wasser in stark exothermer Reaktion zu Phosphorsäure umgesetzt wird.
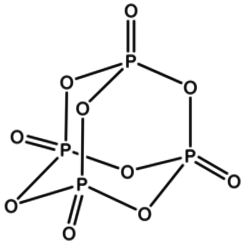
Obwohl lange bekannt ist, dass das Molekül durch die Summenformel P4O10 beschrieben werden kann, ist die historische Bezeichnung (Di)phosphorpentoxid, also P2O5, erhalten geblieben.
Phosphorpentoxid ist auf Grund des vorstehend dargestellten Gleichgewichts ein äußerst wirksames Trocknungsmittel (siehe Exsikkator): Wassermoleküle aus der umgebenden Luft, die auf Phosphorpentoxid treffen, werden sehr stark gebunden. Kommerzielle Trocknungsmittel enthalten 75 % Phosphorpentoxid und 25 % inertes anorganisches Trägermaterial, wodurch eine rieselfähige Struktur des Trocknungsmittels erhalten bleibt. Durch Zusatz von Wasser-Indikatoren wird der Erschöpfungsgrad des Mittels angezeigt. Bei Wasseraufnahme verfärbt sich der ursprünglich farblose Indikator über grün, blaugrün nach blau (Wassergehalt ca. 33 %).
In Gasen, Flüssigkeiten und Feststoffen enthaltenes Wasser hat einen höheren Wasserdampfdruck, wodurch die Wassermoleküle nach und nach fast vollständig zum Phosphorpentoxid wandern. Davon betroffen sind auch chemisch gebundenes Wasser (siehe Kristallwasser) und sogar getrennt gebundene Wasserstoff- und Hydroxygruppen in organischen Molekülen oder biologischem Material: Auch diese haben einen gewissen Wasserdampfdruck, d. h., eine OH-Gruppe bildet mit einem benachbart gebundenen H-Atom gelegentlich ein Wassermolekül, das bei extremer Lufttrockenheit verdunstet. In der uns umgebenden, Wasserdampf enthaltenden Luft spielt dieses Gleichgewicht keine Rolle, aber ein Stück Würfelzucker wird im Exsikkator schwarz wie der im Backofen vergessene Kuchen (dem das Wasser auf dem gleichen Wege durch die Hitze verloren ging).
Düngemittel enthalten Phosphate wie z. B. Kaliumdihydrogenphosphat KH2PO4 oder Diammoniumhydrogenphosphat (NH4)2HPO4, wobei der Gehalt an Phosphor oft auf Phosphorpentoxid (P2O5) umgerechnet angegeben wird.
Zwar wird Phosphorpentoxid in der organischen Chemie praktisch nur als Trocknungsmittel eingesetzt, experimentell konnte jedoch gezeigt werden, dass das Kation von Phosphorpentoxid in der Gasphase so reaktiv ist, dass es sogar die stabilste aller Kohlenstoff-Wasserstoff-Bindungen, und zwar die von Methan, effektiv bei Raumtemperatur aktivieren kann.
Industrielle Verwendung findet die Verbindung zur Herstellung sehr reiner thermischer Phosphorsäure und zur Synthese von organischen Phosphorsäureestern. Die Umsetzung mit Ethern führt zu den Triestern.