Il n'y a aucun article dans votre panier
Acide lactique
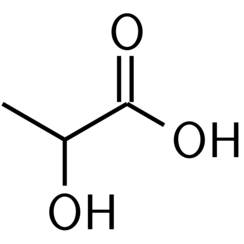
L'acide lactique est un acide organique. Il a la formule moléculaire CH3CH (OH) COOH. Il est blanc à l'état solide et miscible à l'eau. À l'état liquide (état dissous), c'est une solution incolore. La production comprend la synthèse artificielle ainsi que des ressources naturelles. L'acide lactique est un acide alpha-hydroxy (AHA) en raison de la présence d'un groupe hydroxyle à côté du groupe carboxyle. Il est utilisé comme intermédiaire synthétique dans de nombreuses industries de synthèse organique et diverses industries biochimiques. La base conjuguée d'acide lactique est appelée lactate.
En solution, il peut ioniser un proton du groupe carboxyle, produisant l'ion lactate CH 3CH (OH) CO-2. Par rapport à l'acide acétique, le pKa est inférieur d'une unité, ce qui signifie que l'acide lactique est dix fois plus acide que l'acide acétique. Cette acidité plus élevée est due à la liaison hydrogène intramoléculaire entre le groupe α-hydroxyle et le groupe carboxylate.
L'acide lactique est chiral et se compose de deux énantiomères. L'un est connu sous le nom d'acide L - (+) - lactique ou (acide S-lactique et l'autre, son image miroir, est l'acide D - (-) - lactique ou (R) - acide lactique. Un mélange des deux en quantités égales devient DL- appelé acide lactique ou acide lactique racémique. L'acide lactique est hygroscopique. L'acide DL-lactique est miscible à l'eau et à l'éthanol au-dessus du point de fusion, qui est d'environ 16, 17 ou 18 ° C. L'acide D-lactique et l'acide L-lactique ont un point de fusion plus élevé. L'acide lactique est produit par fermentation du lait est souvent racémique, bien que certains types de bactéries ne produisent que de l'acide (R) -lactique. Par contre, l'acide lactique produit par respiration anaérobie dans les muscles des animaux a la configuration (S) et est parfois appelé acide «sarcolactique», du grec "sarx" pour la viande.
Chez les animaux, le L-lactate est constamment produit à partir du pyruvate via l'enzyme lactate déshydrogénase (LDH) au cours d'un processus de fermentation au cours du métabolisme normal et de l'exercice. Il n'augmente pas en concentration jusqu'à ce que le taux de production de lactate dépasse le taux d'élimination du lactate, qui est déterminé par un certain nombre de facteurs, y compris les transporteurs monocarboxylates, la concentration et l'isoforme de LDH, et la capacité oxydative des tissus. La concentration de lactate dans le sang est généralement de 1 à 2 mM au repos, mais peut atteindre plus de 20 mM lors d'un exercice vigoureux, puis 25 mM. Entre autres rôles biologiques, l'acide L-lactique est le principal agoniste endogène du récepteur 1 de l'acide hydroxycarboxylique (HCA1), un récepteur couplé à la protéine G lié à Gi / o (GPCR).
Dans l'industrie, la fermentation de l'acide lactique est réalisée par des bactéries lactiques, qui transforment les glucides simples tels que le glucose, le saccharose ou le galactose en acide lactique. Ces bactéries peuvent également se développer dans la bouche; l'acide qu'ils produisent est responsable de la carie dentaire connue sous le nom de carie dentaire. En médecine, le lactate est l'un des principaux composants de la solution de lactate de Ringer et de la solution de Hartmann. Ces fluides intraveineux sont constitués de cations sodium et potassium ainsi que d'anions lactate et chlorure en solution avec de l'eau distillée, généralement à des concentrations isotoniques avec le sang humain. Il est le plus couramment utilisé pour la réanimation liquidienne après une perte de sang suite à un traumatisme, une intervention chirurgicale ou des brûlures.
L'acide lactique se trouve principalement dans les produits à base de lait aigre, tels que le koumiss, le laban, le yogourt, le kéfir et certains fromages cottage. La caséine du lait fermenté est coagulée (caillée) par l'acide lactique. L'acide lactique est également responsable du goût amer du pain au levain.
Dans les listes d'informations nutritionnelles, l'acide lactique peut être inclus sous le terme «glucides» (ou «glucides par différence»), car il comprend souvent tout sauf l'eau, les protéines, les graisses, les cendres et l'éthanol. Si tel est le cas, l'énergie alimentaire calculée peut utiliser les 4 kilocalories standard (17 kJ) par gramme qui sont souvent utilisées pour tous les glucides. Mais dans certains cas, l'acide lactique est ignoré dans le calcul. La densité énergétique de l'acide lactique est de 362 kilocalories (1 510 kJ) pour 100 g.
Certaines bières (bière aigre) contiennent intentionnellement de l'acide lactique, comme les agneaux belges. Habituellement, cela est produit naturellement par différentes souches de bactéries. Ces bactéries fermentent les sucres en acides, contrairement à la levure qui fermente le sucre en éthanol. Après refroidissement du moût, la levure et les bactéries peuvent "tomber" dans les fermenteurs ouverts. Les brasseurs de styles de bière plus courants empêcheraient ces bactéries de pénétrer dans le digesteur. Les autres styles de bière aigre sont la berliner weisse, la bière rouge flamande et la bière sauvage américaine.
Un processus bactérien naturel ou contrôlé est souvent utilisé dans la vinification pour convertir l'acide malique naturel en acide lactique, pour réduire le piquant et pour d'autres raisons liées à la saveur. Cette fermentation malolactique est réalisée par des bactéries lactiques.
Bien que l'acide lactique ne se trouve normalement pas en quantité significative dans les fruits, c'est le principal acide organique des fruits d'akébie, représentant 2,12% du jus.
En tant qu'additif alimentaire, son utilisation est approuvée dans l'UE, aux États-Unis, en Australie et en Nouvelle-Zélande; il est répertorié sous son numéro INS 270 ou sous le numéro E E270. L'acide lactique est utilisé comme conservateur, durcisseur et aromatisant. C'est un ingrédient dans les aliments transformés et est utilisé comme désinfectant pendant la transformation de la viande. L'acide lactique est produit commercialement par fermentation d'hydrates de carbone tels que le glucose, le saccharose ou le lactose, ou par synthèse chimique. Les sources de glucides comprennent le maïs, les betteraves et le sucre de canne.