Non ci sono articoli nel tuo carrello
Nitrato di manganese (II)
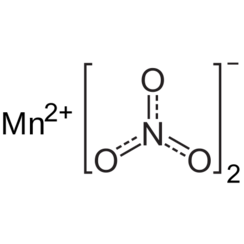
Il nitrato di manganese (II) sono i composti inorganici di formula Mn (NO3) 2 (H2O) n. Ogni unità formula è composta da un catione Mn2 + e due anioni NO3 e diverse quantità di acqua. Il più comune è il tetraidrato Mn (NO3) 2 · 4H2O, ma i mono- ed esaidrati sono anche noti come composti anidri. Alcuni di questi composti sono utili precursori degli ossidi di manganese.
Preparazione, reazioni, applicazioni
Il nitrato di manganese (II) viene preparato sciogliendo l'ossido di manganese (II) in acido nitrico:
MnO + 2 HNO3 → Mn (NO3) 2 + H2O
Può anche essere preparato da biossido di manganese e biossido di azoto:
MnO2 + 2 NO2 → Mn (NO3) 2
Quando riscaldate a 300 ° C, le soluzioni acquose di nitrato di manganese (II) si decompongono termicamente per formare MnO2 e NO2.
Il nitrato di manganese (II) è il precursore del carbonato di manganese, utilizzato nei fertilizzanti e come colorante. Il vantaggio di questo metodo, l'uso di ammoniaca e anidride carbonica, è che il sottoprodotto nitrato di ammonio è utile anche come fertilizzante.