Non ci sono articoli nel tuo carrello
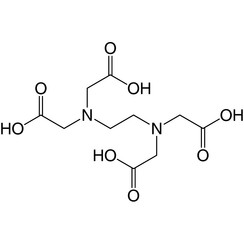
Acido etilendiamminotetraacetico (EDTA)
L'acido etilendiamminotetraacetico (EDTA), noto anche con molti altri nomi, è una sostanza chimica utilizzata sia per scopi industriali che medici. Fu sintetizzato per la prima volta nel 1935 da Ferdinand Münz.
È un acido amminopolicarbossilico e un solido incolore e solubile in acqua. La base coniugata è l'etilendiamminotetraacetato. È ampiamente utilizzato per sciogliere il calcare. La sua utilità deriva dal suo ruolo di legante esadentato ("sei posizioni") e agente chelante, cioè dalla sua capacità di fissare ioni metallici come Ca2 + e Fe3 +. Dopo essere stati legati in un complesso metallico dall'EDTA, gli ioni metallici rimangono in soluzione ma mostrano una reattività ridotta. L'EDTA è prodotto come una varietà di sali, in particolare EDTA disodico, EDTA disodico di calcio e EDTA tetrasodico (tipicamente come idrato).
Applicazioni
-Industria
Nell'industria, l'EDTA viene utilizzato principalmente per immagazzinare ioni metallici in soluzione acquosa. Nell'industria tessile, impedisce ai contaminanti di ioni metallici di alterare i colori dei prodotti tinti. Nell'industria della cellulosa e della carta, l'EDTA inibisce la capacità degli ioni metallici, in particolare Mn2 +, di catalizzare la sproporzione del perossido di idrogeno, che viene utilizzato nello sbiancamento senza cloro. In modo simile, l'EDTA viene aggiunto ad alcuni alimenti come conservante o stabilizzante per prevenire lo scolorimento ossidativo catalitico, che è catalizzato dagli ioni metallici. Nelle bevande analcoliche contenenti acido ascorbico e benzoato di sodio, l'EDTA riduce la formazione di benzene (un agente cancerogeno).
La riduzione della durezza dell'acqua nelle applicazioni di lavaggio e la dissoluzione dei depositi di calcare nelle caldaie si basano entrambi sull'EDTA e sui relativi complessi per legare Ca2 +, Mg2 + e altri ioni metallici. Una volta legati all'EDTA, questi centri metallici tendono a non precipitare né ad interferire con l'azione dei saponi e dei detergenti. Per ragioni simili, le soluzioni detergenti spesso contengono EDTA. In modo simile, l'EDTA viene utilizzato nell'industria del cemento per la determinazione della calce libera e della magnesia libera nel cemento e nel clinker.
La solubilità degli ioni Fe3 + pari o inferiore a pH neutro può essere ottenuta con EDTA. Questa proprietà è utile in agricoltura, compresa l'idroponica. Tuttavia, data la sua dipendenza dal pH dalla formazione del ligando, l'EDTA non è utile per migliorare la solubilità del ferro in terreni sopra neutri. Altrimenti, il ferro (III) si forma a pH quasi neutro e sali insolubili più alti, che sono meno biodisponibili per le specie vegetali sensibili. Acquoso [Fe (EDTA)] - viene utilizzato per rimuovere ("scrub") idrogeno solforato dai flussi di gas. Questa conversione si ottiene ossidando l'idrogeno solforato in zolfo elementare, che è non volatile:
2 [Fe (EDTA)] - + H2S → 2 [Fe (EDTA)] 2− + S + 2 H +
In questa applicazione, il centro del ferro (III) viene ridotto al suo derivato del ferro (II), che può quindi essere riossidato dall'aria. In modo simile, gli ossidi di azoto vengono rimossi dai flussi di gas con [Fe (edta)] 2−. Le proprietà ossidanti del [Fe (edta)] sono sfruttate anche in fotografia, dove viene utilizzato per dissolvere le particelle d'argento.
EDTA è stato utilizzato nella separazione dei metalli lantanidi mediante cromatografia a scambio ionico. Perfezionato da F. H. Spedding et al.Nel 1954, il metodo si basa sul costante aumento della costante di stabilità dei complessi EDTA di lantanidi con numero atomico. Utilizzando perle di polistirene solfonato e Cu2 + come ione di ritenzione, l'EDTA fa sì che i lantanidi migrino lungo la colonna di resina mentre si separano in bande di lantanidi puri. I lantanidi eluiscono in ordine decrescente di numero atomico. A causa del costo di questo metodo, rispetto all'estrazione in controcorrente, lo scambio ionico viene ora utilizzato solo per ottenere la massima purezza dei lantanidi (in genere superiore al 99,99%).
-Medicinale
Un sale specifico di EDTA, noto come sodio calcio edetato, viene utilizzato per legare gli ioni metallici nella pratica della terapia chelante, come per il trattamento del mercurio e dell'avvelenamento da piombo. È usato in modo simile per rimuovere il ferro in eccesso dal corpo. Questa terapia è usata per trattare la complicanza di trasfusioni di sangue ripetute, come sarebbe usata per trattare la talassemia.
Dentisti ed endodontisti utilizzano soluzioni EDTA per rimuovere lo sporco inorganico (strato di sbavatura) e lubrificare i canali radicolari in endodonzia. Questa procedura aiuta a preparare i canali radicolari per l'otturazione. Inoltre, con l'aggiunta di un tensioattivo, le soluzioni EDTA allentano la calcificazione in un canale radicolare e consentono la strumentazione (canalizzazione) e facilitano la progressione apicale di una lima in un canale radicolare stretto o calcificato fino all'apice.
Serve come conservante (di solito per potenziare l'azione di un altro conservante come il benzalconio cloruro o il tiomersale) nelle preparazioni oculari e nei colliri.
Nella valutazione della funzione renale, il complesso di cromo (III) [Cr (edta)] - (come cromo radioattivo-51 (51Cr)) viene somministrato per via endovenosa e viene monitorata la sua filtrazione nelle urine. Questo metodo è utile per valutare la velocità di filtrazione glomerulare (GFR) in medicina nucleare.
L'EDTA è ampiamente utilizzato nell'analisi del sangue. È un anticoagulante per campioni di sangue per CBC / FBE, dove l'EDTA chela il calcio nel campione di sangue, arresta il processo di coagulazione e mantiene la morfologia delle cellule del sangue. Le provette con EDTA sono contrassegnate con boccioli color lavanda o rosa. EDTA è disponibile anche in tubi superiori marrone chiaro per test del piombo e può essere utilizzato in tubi superiori blu reale per test su metalli in tracce.
L'EDTA è un disperdente del muco e ha dimostrato di essere molto efficace nel ridurre la crescita batterica durante l'impianto di lenti intraoculari (IOL).
Medicina alternativa
Alcuni professionisti alternativi ritengono che l'EDTA agisca come antiossidante e impedisca ai radicali liberi di danneggiare le pareti dei vasi sanguigni, riducendo così l'aterosclerosi. Queste idee non sono supportate da studi scientifici e sembrano contraddire alcuni principi attualmente accettati. La FDA statunitense non l'ha approvato per il trattamento dell'aterosclerosi.
-Cosmetici
In shampoo, detergenti e altri prodotti per la cura personale, i sali EDTA vengono utilizzati come agenti sequestranti per migliorare la loro stabilità nell'aria.
-Applicazioni di laboratorio
In laboratorio, l'EDTA è ampiamente utilizzato per il lavaggio degli ioni metallici: in biochimica e biologia molecolare, l'esaurimento ionico viene spesso utilizzato per disattivare gli enzimi dipendenti dal metallo, sia come test della loro reattività che per sopprimere i danni a DNA, proteine e polisaccaridi. L'EDTA agisce anche come inibitore selettivo contro gli enzimi idrolizzanti dNTP (Taq polimerasi, dUTPasi, MutT), arginasi epatica e perossidasi di rafano indipendentemente dalla chelazione degli ioni metallici. Questi risultati sollecitano la riconsiderazione dell'uso dell'EDTA come scavenger di ioni metallici biochimicamente inattivo negli esperimenti enzimatici. In chimica analitica, l'EDTA viene utilizzato nelle titolazioni complessometriche e nell'analisi della durezza dell'acqua o come agente mascherante per isolare gli ioni metallici che interferirebbero con le analisi.
L'EDTA ha molte applicazioni specializzate in laboratori biomedici come l'oftalmologia veterinaria come anticollagenasi per prevenire l'aggravamento delle ulcere corneali negli animali. Nella coltura tissutale, l'EDTA viene utilizzato come agente chelante che si lega al calcio e impedisce l'attaccamento delle caderine tra le cellule, impedisce l'aggregazione delle cellule coltivate in sospensione liquida o allenta il passaggio delle cellule aderenti. In istopatologia, l'EDTA può essere utilizzato come agente disincrostante, consentendo di tagliare sezioni con un microtomo una volta che il campione di tessuto è stato demineralizzato. L'EDTA è anche noto per inibire una serie di metallopeptidasi, il metodo di inibizione avviene attraverso la chelazione dello ione metallico necessario per l'attività catalitica. L'EDTA può anche essere utilizzato per testare la biodisponibilità dei metalli pesanti nei sedimenti. Tuttavia, può influenzare la biodisponibilità dei metalli in soluzione, il che può sollevare preoccupazioni sui suoi effetti sull'ambiente, soprattutto dati i suoi usi e applicazioni diffusi.