U heeft geen artikelen in uw winkelwagen
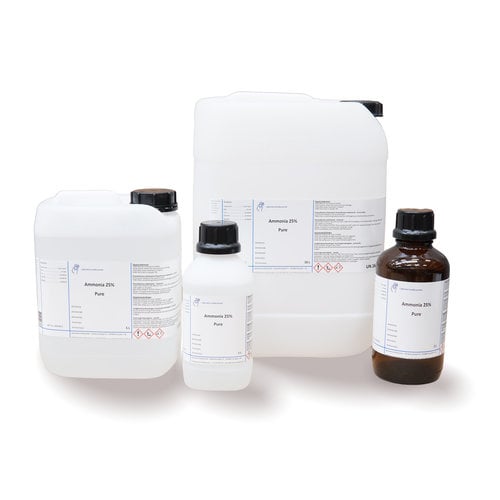
Ammonia 25%, puur
- Bestel 2 en bespaar 5%
- Bestel 6 en bespaar 10%
Wat is ammonia?
Ammoniak of Ammonia wanneer het in water is opgelost. is een chemische verbinding van stikstof en waterstof met de empirische formule NH3. Het is een kleurloos, in water oplosbaar en giftig gas met een sterke penetrante geur die tranen veroorzaakt en verstikkend is. Ammoniak is een amfotere stof: onder waterige omstandigheden fungeert het als basis. Het vormt verschillende series zouten: zowel de kationogene ammoniumzouten als de anionogene amiden, imiden en nitriden waarin één (amide), twee (imiden) of alle (nitriden) protonen (waterstofionen) zijn vervangen door metaalionen.
Ammoniak is een van de meest geproduceerde chemicaliën en basismateriaal voor de productie van alle andere stikstofverbindingen. De meeste ammoniak wordt verwerkt tot meststoffen, vooral ureum en ammoniumzouten. Tot dusver (2020) werd vrijwel uitsluitend geproduceerd met behulp van het Haber-Bosch-proces uit de elementen waterstof en stikstof.
Biologisch gezien heeft ammoniak een belangrijke functie als tussenproduct bij de vorming en afbraak van aminozuren. Door de toxiciteit van grotere hoeveelheden ammoniak wordt het omgezet in niet-giftig ureum of, bijvoorbeeld bij vogels, in urinezuur voor uitscheiding in het lichaam.
-Toepassingen
-Basismateriaal voor de productie van alle andere industrieel geproduceerde stikstofhoudende verbindingen
Met een aandeel van 40% in 1995 is ureum de belangrijkste verbinding die wordt geproduceerd uit ammoniak, dat voornamelijk wordt gebruikt als meststof en voor de productie van ureumharsen; Ureum wordt verkregen door ammoniak te laten reageren met kooldioxide.
Naast ureum worden er ook andere stikstofhoudende meststoffen gemaakt van ammoniak. De belangrijkste zijn de ammoniumzouten ammoniumnitraat, fosfaat en sulfaat. In totaal bedroeg het aandeel van meststoffen in het totale ammoniakverbruik in 2003 83%.
Een andere belangrijke stof die uit ammoniak wordt gemaakt, is salpeterzuur, dat op zijn beurt het uitgangsmateriaal is voor een groot aantal andere verbindingen. In het Ostwald-proces reageert ammoniak met zuurstof op platina-mazen en vormt zo stikstofoxiden, die met water reageren en salpeterzuur vormen.
-Rol in verschillende organische syntheses
Primaire carboxamiden kunnen worden verkregen uit ammoniak en geschikte carbonzuurderivaten zoals carbonzuurchloriden of esters. Daarentegen vindt de directe reactie van carbonzuur en ammoniak om het overeenkomstige amide te vormen alleen plaats bij verhoogde temperaturen wanneer het eerder gevormde ammoniumzout ontleedt. Een technisch belangrijke reactie is die van adipinezuur en ammoniak om adipinezuurdinitril te vormen. Dit wordt verder gehydrogeneerd tot hexamethyleendiamine, waardoor het een tussenproduct wordt voor de vervaardiging van nylon.
Het is mogelijk om aniline te produceren door de reactie van fenol en ammoniak op een aluminiumsilicaatkatalysator. Deze synthetische route vereist echter meer energie en geeft een lagere opbrengst dan de synthese en reductie van nitrobenzeen en wordt daarom slechts in beperkte mate gebruikt wanneer fenol goedkoop verkrijgbaar is.
-Speciale toepassingen
De reactie van ammoniak met zuren wordt gebruikt bij de rookgasreiniging. Het is in staat om te reageren met zwavelzuur en salpeterzuur en verwijdert zo ongewenste, milieubelastende zwavel- en stikstofoxiden uit het rookgas.
Vanwege zijn grote specifieke verdampingsenthalpie van 1368 kJ / kg wordt ammoniak ook als koelmiddel gebruikt. Voordelen zijn lage brandbaarheid, de niet bestaande bijdrage aan het broeikaseffect of de vernietiging van de ozonlaag en het toepassingsbereik van −60 tot +100 ° C. De toxiciteit van de verbinding is nadelig.
Ammoniakoplossing wordt ook gebruikt in olfactorische ampullen. De extreme geurprikkel dient als een anti-dissociatieve strategie, bijvoorbeeld in de context van dialectische gedragstherapie.
Ammoniak reageert met het looizuur dat in hout wordt aangetroffen en kleurt het hout donkerbruin afhankelijk van de concentratie van het looizuur. Eikenhout wordt bijvoorbeeld met ammoniak of salmiak getransformeerd tot het donkerbruine gerookte eikenhout. Ammoniak wordt ook gebruikt om te kleuren bij de productie van blauwdrukken (diazotypes).
Er zijn ook experimentele brandstofcelsystemen waarin de benodigde waterstof wordt verkregen wanneer deze nodig is door de ammoniak te splitsen met behulp van chemische processen. Een andere benadering die is onderzocht, is om ammoniak te gebruiken als een gemakkelijk te hanteren opslagapparaat voor chemische energie, bijvoorbeeld om overtollige elektriciteit uit fluctuerende hernieuwbare energiebronnen (wind- en zonne-energie) op lange termijn en op industriële schaal op te slaan , om hiaten in de levering van deze energieën te dichten en om Gebruik hernieuwbare energiebronnen voor de voortstuwing van voertuigen, bijvoorbeeld in scheepsmotoren. Door het rendement van ca. 55-60% bij het omzetten van elektrische energie in chemische energie van ammoniak en terug in grote diesel- of gecombineerde cyclus energiecentrales (samen ca. 2/3 energieverliezen) is dit echter beduidend minder energetisch dan het direct gebruik van hernieuwbare energiebronnen voor de dekking van de elektriciteitsvraag.
Ammonia kopen?
Laboratoriumdiscounter verkoopt ammonia in verschillende verpakkingen en voor een vriendelijke prijs! U besteld dus uw ammonia snel en makkelijk via Laboratoriumdiscounter.nl. Snel verzonden!
Technische gegevens:
Ammonium hydroxide solution, Salmiac solution
Empirical formula NH3 + H2O
Molar mass (M) 17,03 + aq g/mol
ADR 8 III
WGK 2
CAS No. [1336-21-6]
EG-Nr. 215-647-6
UN-Nr. 2672
Downloads
$$$$$
Gevarenaanduidingen
H290 Kan bijtend zijn voor metalen
H314 Veroorzaakt ernstige brandwonden en oogletsel
H335 Kan irritatie van de luchtwegen veroorzaken
H400 Zeer giftig voor in het water levende organismen
Veiligheidsaanbevelingen
Voorzorgsmaatregelen - preventie
P273 Voorkom lozing in het milieu.
P280 Beschermende handschoenen/beschermende kleding/oogbescherming/gelaatsbescherming dragen.
Voorzorgsmaatregelen - reactie
P303+P361+P353 BIJ CONTACT MET DE HUID (of het haar): verontreinigde kleding onmiddellijk
uittrekken. Huid met water afspoelen [of afdouchen].
P305+P351+P338 BIJ CONTACT MET DE OGEN: voorzichtig afspoelen met water gedurende een
aantal minuten; contactlenzen verwijderen, indien mogelijk; blijven spoelen.
P310 Onmiddellijk een ANTIGIFCENTRUM/arts raadplegen.