U heeft geen artikelen in uw winkelwagen
Aluminiumsulfaat
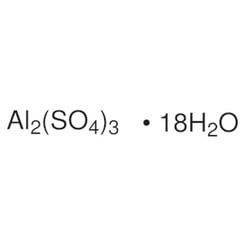
Aluminiumsulfaat is een chemische verbinding met de formule Al2(SO4)3. Het is oplosbaar in water en wordt voornamelijk gebruikt als coagulatiemiddel (het bevorderen van de botsing van deeltjes door de lading te neutraliseren) bij de zuivering van drinkwater en afvalwaterzuiveringsinstallaties, en ook bij de papierproductie.
De watervrije vorm komt van nature voor als een zeldzaam mineraal millosevichiet, dat b.v. in vulkanische omgevingen en bij het verbranden van stortplaatsen voor steenkoolwinning. Aluminiumsulfaat wordt zelden of nooit aangetroffen als het watervrije zout. Het vormt een aantal verschillende hydraten, waarvan hexadecahydraat Al2 (SO4) 3 • 16H2O en octadecahydraat Al2 (SO4) 3 • 18H2O het meest voorkomen. Het heptadecahydraat, waarvan de formule kan worden geschreven als [Al (H2O) 6] 2 (SO4) 3 • 5H2O, komt van nature voor als het minerale alunogeen.
Aluminiumsulfaat wordt in bepaalde industrieën soms aluin genoemd. De naam "aluin" wordt echter vaker en beter gebruikt voor elk dubbel sulfaatzout met de generieke formule XAl(SO4)2 · 12H
2O, waarbij X een eenwaardig kation is zoals kalium of ammonium.
Toepassingen
Het wordt soms gebruikt in de voedingsindustrie als verstevigingsmiddel, waar het E-nummer E520 aanneemt, en in diervoeder als bactericide. Aluminiumsulfaat kan worden gebruikt als deodorant, bindmiddel of als stipticum voor oppervlakkige scheerwonden.
Het is een veelvoorkomend vaccinadjuvans en werkt "door de langzame afgifte van antigeen uit het vaccindepot op de inoculatieplaats te vergemakkelijken".
Aluminiumsulfaat wordt gebruikt bij waterzuivering en als bijtmiddel bij het verven en bedrukken van textiel. Bij waterzuivering zorgt het ervoor dat zwevende onzuiverheden tot grotere deeltjes coaguleren en zich dan gemakkelijker op de bodem van de container nestelen (of worden uitgefilterd). Dit proces wordt coagulatie of flocculatie genoemd. Onderzoek wijst uit dat aluminiumsulfaat dat op deze manier wordt gebruikt bij de behandeling van drinkwater in Australië de belangrijkste bron is van waterstofsulfidegas in rioleringen. Een onjuist en buitensporig toepassingsincident in 1988 vervuilde de watervoorziening van Camelford in Cornwall.
Wanneer aluminiumsulfaat wordt opgelost in een grote hoeveelheid neutraal of licht alkalisch water, ontstaat er een gelatineus neerslag van aluminiumhydroxide, Al(OH)3. Bij het verven en bedrukken van textiel helpt het gelatineuze neerslag de kleurstof te hechten aan de kledingvezels door het pigment onoplosbaar te maken.
Aluminiumsulfaat wordt soms gebruikt om de pH van tuingrond te verlagen, omdat het hydroliseert om het aluminiumhydroxideprecipitaat en een verdunde zwavelzuuroplossing te vormen. Een voorbeeld van wat het veranderen van de pH-waarde van aarde voor planten kan doen, is zichtbaar als je naar Hydrangea macrophylla kijkt. De tuinman kan aluminiumsulfaat aan de grond toevoegen om de pH te verlagen, waardoor de bloemen van de hortensia een andere kleur (blauw) krijgen. Het aluminium is wat de bloemen blauw maakt; bij een hogere pH is het aluminium niet beschikbaar voor de plant.
In de bouw wordt het gebruikt als waterdichtingsmiddel en versneller in beton. Een ander gebruik is een schuimmiddel in blusschuim.
Het kan ook zeer effectief zijn als slakkenbestrijdingsmiddel, waarbij Spaanse slakken worden gedood.
Beitsen van aluminiumtriacetaat en aluminiumsulfacetaat kunnen worden bereid uit aluminiumsulfaat, waarbij het gevormde product wordt bepaald door de hoeveelheid gebruikt lood(II)acetaat